生命学院杨雪瑞课题组开发单细胞剪接谱分析工具,提出解读复杂组织细胞异质性的新思路

生命学院杨雪瑞课题组
开发单细胞剪接谱分析工具
提出解读复杂组织细胞异质性的新思路
全文约2500字,阅读约8分钟。
大多数生理和病理组织都表现出显著的细胞异质性,即在同一组织或群体中,不同细胞之间在形态、功能、基因表达等方面存在差异和多样性。对这些细胞异质性的系统性解读,特别是精准鉴定具有关键功能的细胞群体(亚型),对于理解组织器官的发育及功能、细胞互作微环境、疾病的动态发展等生理与病理过程具有重要价值。当前主流的细胞异质性分析以单细胞转录组分析为基础,通过对单个细胞中的mRNA进行测量,获得复杂组织中每个细胞的基因表达谱,以定义不同的细胞群体,构建复杂组织中的细胞异质性谱图。然而,这一经典的分析方法仅局限于基因层面,无法提供基因转录本的详细信息,几乎完全忽略了RNA可变剪接在塑造生理状态、执行生物学功能以及推动疾病发展过程中的关键作用。
在高等真核生物中,RNA可变剪接是一种重要的基因转录后调控机制。细胞内的DNA首先被转录为RNA,再经过复杂的转录后加工,形成编码蛋白质的mRNA。通过改变基因的剪接模式,一个基因可以生成多个不同的mRNA转录本,从而极大地增加了转录组和蛋白组的复杂性,体现了基因表达和功能的多样性和可塑性。然而,传统的单细胞基因表达谱数据仅能反映基因整体表达水平,无法揭示转录后RNA剪接这一重要调控层级。因此,为了更全面地理解复杂组织中的细胞异质性,我们需要补足RNA剪接谱这一关键维度的信息缺失,从而更加深入和系统地衡量生理及病理组织中细胞的状态和功能和相互作用。
针对这一关键需求,清华大学生命学院杨雪瑞课题组开发了生物信息工具SCASL (single-cell clustering d on alternative splicing landscapes),用于单细胞RNA剪接谱异质性的系统、定量分析,基于剪接谱重新定义细胞亚群。该研究成果于3月9日发表于《自然通讯》(Nature Communications),文章标题为“使用SCASL对单细胞RNA剪接谱的解析提出了具有生理学意义的细胞身份新定义”(Interrogations of single-cell RNA splicing landscapes with SCASL define new cell identities with physiological relevance)。

图1. 论文在线发表首页
SCASL方法使用单细胞RNA测序数据,在不依赖于转录组注释(已预先定义的转录本信息等)的前提下,对不同的可变剪接模式进行定量,计算单细胞内不同选择性剪接事件的概率。以此为基础,SCASL通过kNN方法对剪接谱中的缺失值进行了多次的迭代估算和填补,解决了由于技术及样本限制导致的单细胞RNA剪接数据覆盖不均匀与高稀疏性问题。最后,SCASL使用基于图的无监督聚类算法——谱聚类,对细胞亚型进行了分类,从而绘制单细胞RNA剪接异质性图谱。测试结果显示,SCASL在对缺失值的估算准确性、细胞聚类结果的稳定性、稀有细胞类群鉴定、随机噪音容忍度等方面均表现出色,这也体现出单细胞剪接谱所包含信息的高冗余度。重要的是,基于相同的单细胞RNA-seq数据,SCASL利用剪接谱信息对细胞身份的定义与仅仅基于基因表达谱的细胞聚类结果有显著差异。
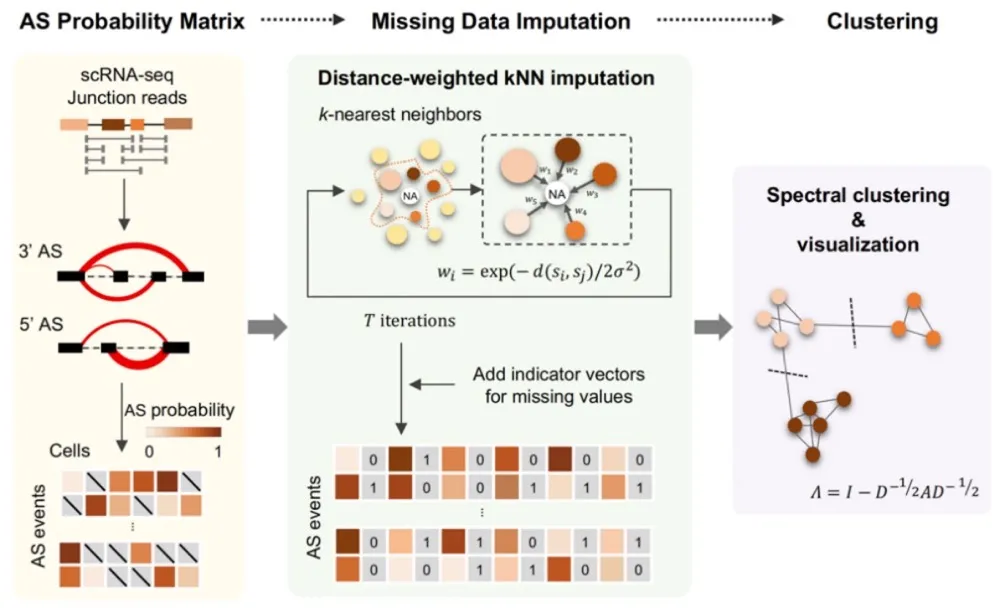
图2. SCASL分析流程概念示意图
进一步,作者使用了七套已发表的单细胞RNA-seq数据,对SCASL剪接谱异质性分析结果的生物学意义进行了深入挖掘和讨论。
细胞异质性对于肿瘤的发展、转移和治疗具有重要影响。它可以导致肿瘤内部的细胞亚群具有不同的增殖能力、耐药性和转移能力,从而增加肿瘤的侵袭性和复发风险。此外,细胞异质性也使得某些肿瘤细胞亚群对特定治疗方法更具抗药性,从而限制了肿瘤治疗的有效性。三阴性乳腺癌是由正常乳腺上皮细胞发展的一种乳腺癌亚型,其特点是缺乏雌激受体表达,限制了常规激素和靶向治疗的应用,相对于其他乳腺癌通常具有更高的肿瘤复发率和更差的预后。通过对三阴性乳腺癌细胞剪接谱异质性的分析,SCASL明确定义了正常上皮细胞的癌前发展状态、早期肿瘤细胞、恶性肿瘤细胞及微转移肿瘤细胞簇。特别值得注意的是,在与健康细胞的相关分析中,剪接谱显示了健康细胞与早期和晚期肿瘤细胞簇之间的过渡特征,而表达谱无法展示这一点。事实上,由于肿瘤细胞高度的异质性,特别是基因表达谱的无序扰动(肿瘤细胞中重塑的基因表达谱具有更大的不确定性和变动性),此前对肿瘤单细胞基因表达谱的聚类通常不够稳定,难以明确定义细胞亚型及其边界。SCASL的分析结果表明RNA剪接谱对于定义细胞亚型,特别是过渡态细胞,具有独特优势,表明RNA可变剪接在驱动肿瘤发生发展中潜在的重要作用。
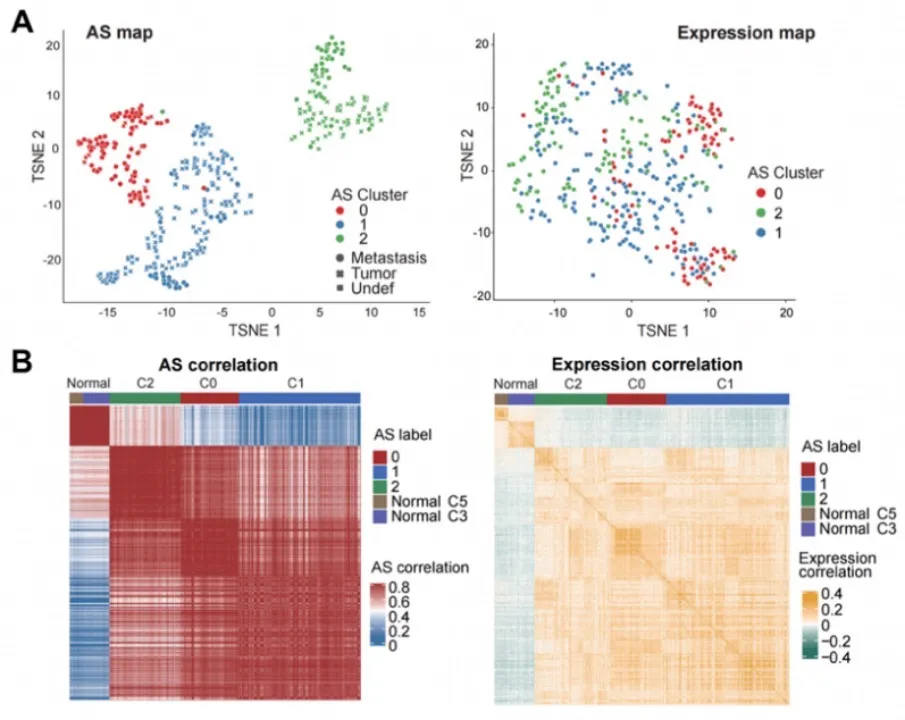
图3. (A) 三阴性乳腺癌细胞的聚类可视化和 (B) 肿瘤细胞与健康细胞的相关性分析,分别基于剪切谱(左)和表达谱(右)。C2是早期肿瘤细胞亚型,C0是微转移细胞亚型,C1是晚期肿瘤细胞亚型。
在对正常组织发育动态过程的解读中,SCASL也表现出独特的优势。例如,SCASL重现了小鼠胚胎肝脏中肝母细胞发育为肝细胞和胆管细胞的两个谱系,明确定义了分化谱系中的时序过渡态细胞。更有趣的是,SCASL基于剪接谱的分析揭示了一个特殊的细胞簇,它此前被定义为胆管细胞,但其剪接谱位于肝细胞和胆管细胞两个发育谱系之间,且同时表现出两种细胞的功能特征,表明其可能代表了肝脏发育过程中两个细胞分化路径之间的交流。
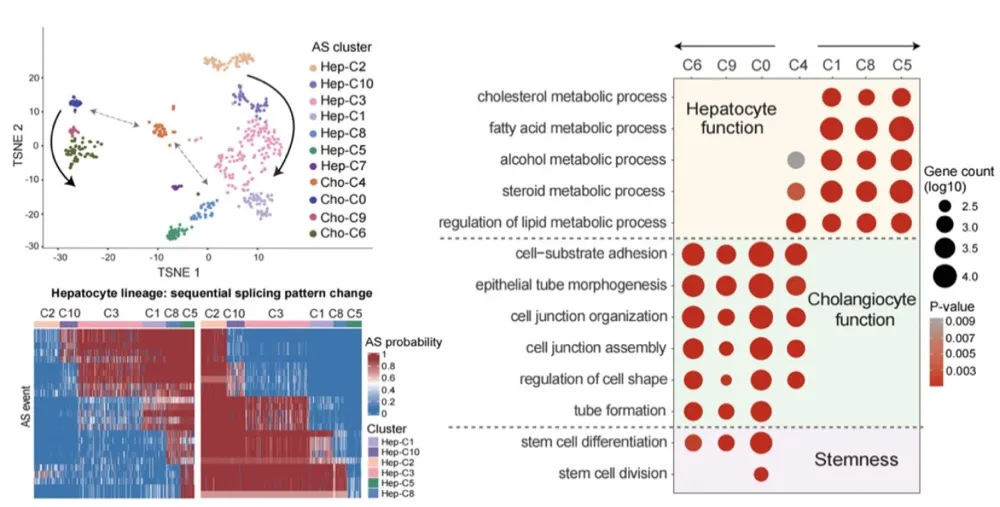
图4. SCASL重现小鼠胚胎肝细胞发育谱系(左),发现肝细胞和胆管细胞两个谱系间的中间态细胞(右)
最后,在对肿瘤免疫微环境的分析中,SCASL完成了对肿瘤相关T细胞亚型的精细鉴定,包括肿瘤浸润的耗竭型、激活型CD8 T细胞、不同功能活性的CD4 T细胞等。同时,通过耗竭亚型的差异剪切分析,作者还得到了许多重要的差异剪切事件,其中一些事件已经被大量研究证明的确会促进CD8 T细胞的耗竭。以上新的细胞身份定义为理解免疫细胞浸润、激活与耗竭、细胞互作调控等重要过程提供了新的线索,特别是重要基因的RNA可变剪接对肿瘤免疫微环境的塑造。
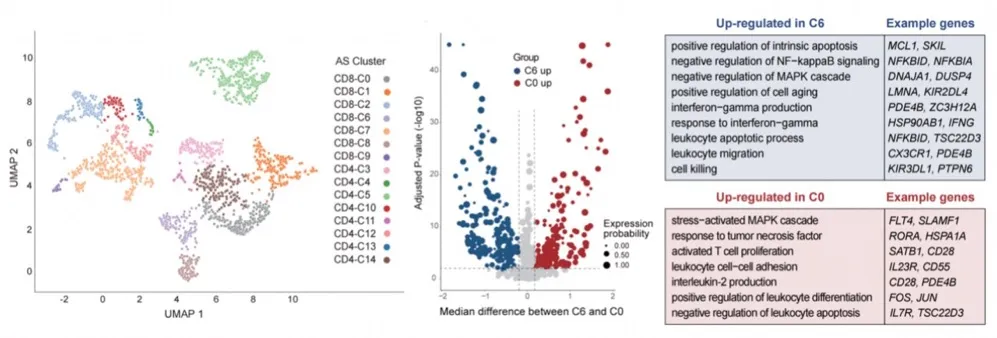
图5. T细胞剪接谱聚类可视化(左)及肿瘤浸润CD8 T细胞簇的差异表达功能富集(右),C6相对于C0呈现出非常显著的耗竭特征。
总之,本项工作为复杂组织中细胞异质性的解读提出了新的视角与方法。通过这一技术的应用,本研究深入分析了多个重要的生物学过程,提出一系列新观察、新线索与新发现。清华大学生命学院2019级博士生向贤珂为论文第一作者,杨雪瑞副教授为论文通讯作者。北京大学生物医学前沿创新中心张泽民教授及团队成员何尧博士为本研究提供了数据、工具等方面的重要贡献。本工作得到国家重点研发计划、国家自然科学基金委、国家高层次人才特殊支持计划、清华大学的资助。国家蛋白质科学研究(北京)设施(清华大学蛋白质研究技术中心)下属生物计算平台、基因测序与分析平台为本研究提供了大力支持。
>>详情请参阅【论文原文】
https://www.nature.com/articles/s41467-024-46480-9
(由于篇幅原因,参考文献未能展现)
作者信息

杨雪瑞

张泽民
向贤珂,清华大学生命学院2019级博士生
杨雪瑞,清华大学生命科学学院副教授;主要研究方向为基因组学与癌症系统生物学。
张泽民,北京大学生物医学前沿创新中心(BIOPIC)主任,北京大学生命科学学院讲席教授,北大清华联合中心高级研究员。张泽民实验室致力于用前沿的基因组学和生物信息学技术来解决癌症生物学中的重要问题,结合计算(干)和实验(湿)方法来揭示肿瘤发生过程、微环境和对药物响应中的系统变化和具体遗传因素,以推进癌症免疫治疗和靶向治疗的发展。
何 尧,北京大学前沿交叉学院博士生

